Feuerfester Power-Akku wird wahrscheinlicher
Neuer Hochleistungselektrolyt von ANL und University of Waterloo erfüllt höchste Erwartungen
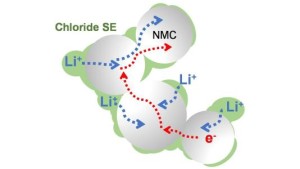 |
Schematische Darstellung des neuen Festkörperelektrolyten (Illustration: Linda Nazar, uwaterloo.ca) |
Lemont/Waterloo (pte001/12.05.2022/06:00)
Der Weg zu einer leistungsfähigen Lithium-Ionen-Batterie, die weder explodieren noch brennen kann, ist geebnet. Forscher des Argonne National Laboratory (ANL) http://www.anl.gov , das vom US-Energieministerium betrieben wird, und der University of Waterloo http://uwaterloo.ca haben einen Festkörperelektrolyten aus Lithium, Scandium, Indium und Chlor entwickelt, der Lithiumionen gut, Elektronen aber schlecht leitet. Das ist die Voraussetzung dafür, dass die damit ausgestattete Batterie eine hohe Kapazität hat und hunderte Lade- und Entladezyklen übersteht, ohne nennenswert an Kapazität zu verlieren.
Scandium statt Indium
Der Elektrolyt trennt die beiden Elektroden (Anode und Kathode) voneinander. Er hat die Aufgabe zu isolieren und Lithium-Ionen beim Laden und Entladen passieren zu lassen. Am besten klappt das mit flüssigen Elektrolyten, doch die können Feuer fangen, wenn es zu einem Kurzschluss kommt. Der wird oft von sogenannten Dendriten ausgelöst, Lithium-Ablagerungen auf einer Elektrode, die nadelspitz sind und den Elektrolyten durchstoßen können. Festkörperelektrolyte sind dagegen undurchdringlich.
"Die Hauptattraktion eines Festkörperelektrolyten besteht darin, dass er kein Feuer fangen kann", sagt Linda Nazar von der University of Waterloo, die auch dem ANL angehört. Nazars Gruppe ist nicht die erste, die einen Chloridelektrolyten entwickelt. Doch der neue Elektrolyt übertrifft eigenen Angaben nach alle bisherigen Vorgänger, weil die Forscher die Hälfte des Indiums gegen Scandium ausgetauscht haben. Das hat für eine bessere Ionen- und schlechtere Elektronenleitfähigkeit geführt, wie es heißt.
"Wie Tanzveranstaltung"
Ein chemischer Schlüssel zur Ionen-Leitfähigkeit liegt in der Kristallstruktur, die der eines natürlich vorkommenden Minerals namens Spinell ähnelt. Bei der Komposition des neuen Elektrolyten mussten die Forscher zwei konkurrierende Faktoren ausbalancieren: Die Spinellstruktur mit so vielen Ionen wie möglich zu beladen, aber auch Stellen offen zu lassen, durch die sich die Ionen bewegen können. "Man kann das mit einer Tanzveranstaltung vergleichen. Sie möchten, dass viele Leute kommen, aber es soll nicht zu voll werden", so Nazar. Hier die Balance zu finden, sei die entscheidende Aufgabe gewesen.
(Ende)| Aussender: | pressetext.redaktion |
| Ansprechpartner: | Wolfgang Kempkens |
| Tel.: | +43-1-81140-300 |
| E-Mail: | kempkens@pressetext.com |
| Website: | www.pressetext.com |